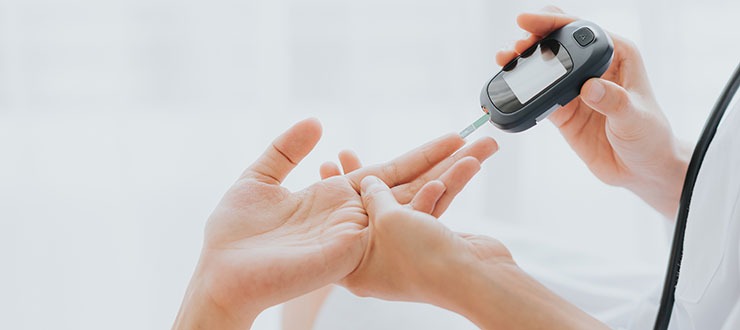
La Commission européenne a autorisé, lundi 12 janvier 2026 la mise sur le marché de Teizeild, un traitement innovant de Sanofi destiné aux adultes et enfants de plus de 8 ans atteints de diabète de type 1 au stade 2. Ce traitement, déjà approuvé aux États-Unis, au Royaume-Uni et en Chine depuis 2022, offre une option préventive avant l’apparition des symptômes cliniques.
Teizeild est un anticorps monoclonal administré par perfusion intraveineuse sur 12 jours. Il agit en modulant le système immunitaire et en ciblant les lymphocytes T CD3, ralentissant la progression de la maladie. Les résultats de l’étude pivot TN-10 ont montré qu’après traitement, 57 % des patients restaient au stade 2 contre 28 % sous placebo, prolongeant ainsi l’indépendance à l’insuline.

Selon Olivier Charmeil, vice-président de Sanofi, cette approbation offre une option préventive à des milliers de patients en Europe et transforme le paradigme thérapeutique du diabète de type 1. Des études supplémentaires seront menées pour évaluer l’impact à long terme sur les complications de la maladie.
Le diabète de type 1 est une maladie auto-immune où le système immunitaire détruit les cellules bêta du pancréas, entraînant une hyperglycémie. Détecté tôt au stade préclinique grâce au dépistage, Teizeild permet d’intervenir avant que la fonction des cellules bêta ne soit trop altérée.